行業(yè)動態(tài)
您當前的位置 > 行業(yè)動態(tài) > 行業(yè)新聞
廣東省近7萬款醫(yī)療器械賦碼,多地UDI實施進程一覽
加入日期:2021/12/17 9:36:37 查看人數(shù): 1906 作者:admin
近日,廣東省藥品監(jiān)管局在深圳市召開推進醫(yī)療器械唯一標識系統(tǒng)試點工作現(xiàn)場會,現(xiàn)階段性總結醫(yī)療器械唯一標識系統(tǒng)試點工作進展和成效。
截至12月3日,廣東省有276 家企業(yè)向醫(yī)療器械唯一標識數(shù)據(jù)庫填報數(shù)據(jù)69669條,有236家企業(yè)發(fā)布數(shù)據(jù)67444條,其中三類企業(yè)有130家已填報數(shù)據(jù),110家已發(fā)布數(shù)據(jù)。
醫(yī)療器械唯一標識(Unique Device Identification,簡稱UDI)是醫(yī)療器械產品的電子身份證,可實現(xiàn)全生命周期醫(yī)療器械通查通識,是目前醫(yī)療器械追溯管理最好的方法,在國際上被廣泛使用。
我國UDI試點工作于2019年開始啟動,2021年1月1日首批高風險第三類醫(yī)療器械中9大類69個醫(yī)療器械品種正式實施唯一標識。
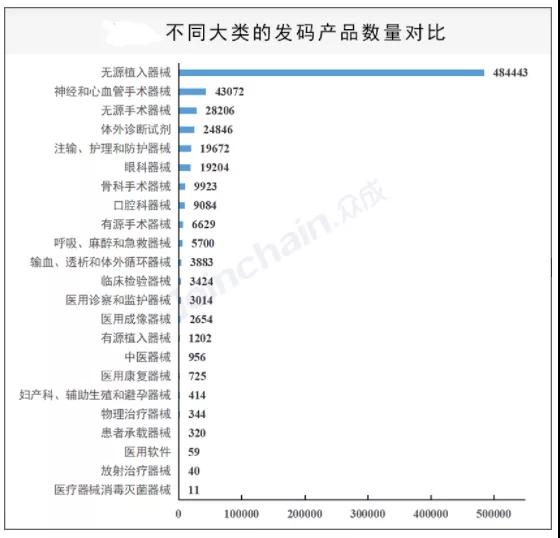
眾成數(shù)科數(shù)據(jù)顯示,自實施以來已有超過60萬醫(yī)療器械產品實施并具有唯一標識,其中絕大部分產品為耗材產品,尤其是無源植入器械,神經和心血管手術器械和無源手術器械,且多為Ⅲ類產品。
為了盡快實現(xiàn)醫(yī)療器械的可追溯,不少省市已提前布局,加快推進UDI的實施。目前,部分省市已經提前完成UDI實施工作,還有部分省市結合實際情況擴大了實施范圍。
四川省藥監(jiān)局在推進UDI工作節(jié)點上明確,2021年9月-11月完成全三類醫(yī)療器械產品賦碼、數(shù)據(jù)上傳和維護等工作。2021年12月,對納入實施企業(yè)和單位完成情況進行檢查驗收。
河北省藥監(jiān)局則要求2021年11月1日起生產的醫(yī)療器械(全三類)應當具有醫(yī)療器械唯一標識。
山東省藥監(jiān)局預計在11月底前轄區(qū)內第三類醫(yī)療器械生產企業(yè)將全部實施UDI。
另外,不少省市在《關于深入推進試點做好第一批實施醫(yī)療器械唯一標識工作的公告》的要求下,結合本地實際情況,擴大了實施范圍,福建、云南、海南、天津等省市將第二類醫(yī)療器械納入實施品種中。
隨著UDI實施范圍不斷擴大,各地工作陸續(xù)推進,將有利于加強我國醫(yī)療器械全生命周期管理,提高醫(yī)療器械識別的準確性和一致性,提升醫(yī)療器械管理水平和效能,有力保障公眾用械安全有效。